新聞資訊 了解首宏動(dòng)態(tài)、掌握行業(yè)資訊
需求。巨大的市場(chǎng)潛力和多方的政策支持,推動(dòng)了我國(guó)醫(yī)療設(shè)備外貿(mào)代理行業(yè)由小到大的快速增長(zhǎng),產(chǎn)品品類(lèi)不斷
提升,創(chuàng)新能力增強(qiáng),部分細(xì)分行業(yè)龍頭企業(yè)。
不可忽視的是,我國(guó)醫(yī)療器械外貿(mào)代理小、多、散和低水平競(jìng)爭(zhēng)的現(xiàn)象尚沒(méi)有得到根本轉(zhuǎn)變,加速技術(shù)創(chuàng)新能力、
加強(qiáng)科學(xué)監(jiān)管是當(dāng)務(wù)之急。
信號(hào)一:創(chuàng)新產(chǎn)品審評(píng)審批將加快
會(huì)議明確,2022年要全面實(shí)施醫(yī)療器械審評(píng)審批電子化,加快創(chuàng)新產(chǎn)品審評(píng)審批;開(kāi)展醫(yī)療器械“線上清網(wǎng)線下規(guī)范
”治理,加大對(duì)疫情防控醫(yī)療器械抽檢力度。
國(guó)家藥品監(jiān)督管理局黨組成員、副局長(zhǎng)徐景和指出,當(dāng)前,我國(guó)醫(yī)療器械行業(yè)進(jìn)入“黃金發(fā)展期”,審評(píng)制度和審批
改革創(chuàng)新已進(jìn)入“深度推進(jìn)期”,監(jiān)管能力建設(shè)進(jìn)入“全面加強(qiáng)期”。監(jiān)管進(jìn)入“高風(fēng)險(xiǎn)期”。
徐景和對(duì)醫(yī)療器械監(jiān)管提出五點(diǎn)要求:深入調(diào)查,整改隱患;繼續(xù)加強(qiáng)對(duì)防疫隊(duì)伍的監(jiān)管;繼續(xù)深化審批制度改革;
全面推進(jìn)風(fēng)險(xiǎn)管理責(zé)任落實(shí),千方百計(jì)加強(qiáng)基礎(chǔ)設(shè)施建設(shè)。
會(huì)議明確,2022年全力支持醫(yī)療器械產(chǎn)業(yè)高質(zhì)量創(chuàng)新發(fā)展。加快創(chuàng)新產(chǎn)品審評(píng)審批,促進(jìn)科技成果轉(zhuǎn)化應(yīng)用,落實(shí)國(guó)
家重大戰(zhàn)略,支持重點(diǎn)地區(qū)產(chǎn)業(yè)發(fā)展。
國(guó)務(wù)院辦公廳去年9月下發(fā)的《“十四五”全民醫(yī)療保障規(guī)劃》號(hào)(以下簡(jiǎn)稱(chēng)《醫(yī)療保障規(guī)劃》號(hào))提出,要提高藥品
供應(yīng)安全。深化審評(píng)審批制度改革,鼓勵(lì)創(chuàng)新藥物開(kāi)發(fā),加快新藥好藥上市,促進(jìn)群眾急需的新藥、醫(yī)療器械開(kāi)發(fā)和
使用。
國(guó)家食品藥品監(jiān)督管理總局在2021年醫(yī)療器械報(bào)告中指出,2021年國(guó)家食品藥品監(jiān)督管理局將繼續(xù)按照《創(chuàng)新醫(yī)療器
械特別審查程序》 《醫(yī)療器械優(yōu)先審批程序》審查相關(guān)產(chǎn)品,共受理醫(yī)療器械創(chuàng)新專(zhuān)項(xiàng)審批申請(qǐng)249件,同比增長(zhǎng)比
2020年增長(zhǎng)26.4%,其中獲批進(jìn)入專(zhuān)項(xiàng)審評(píng)程序62件,受理優(yōu)先申請(qǐng)41件,比2020年增長(zhǎng)46.3%,其中獲批優(yōu)先審批
14件。
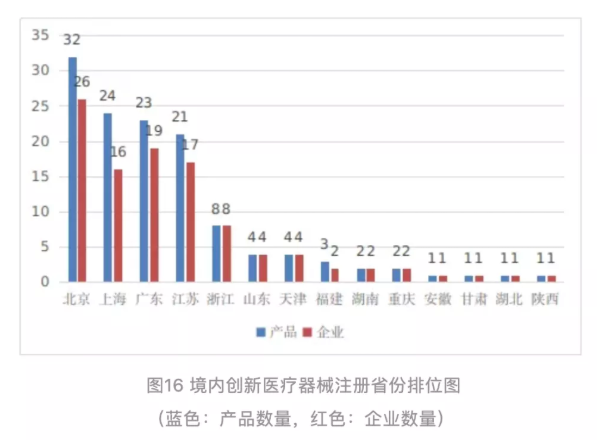
北京、上海、廣東、江蘇、浙江創(chuàng)新醫(yī)療器械獲批產(chǎn)品數(shù)量和相應(yīng)企業(yè)數(shù)量最多,約占全部已批準(zhǔn)的134個(gè)創(chuàng)新醫(yī)療器
械的81%。
信號(hào)二:全面落實(shí)注冊(cè)人制度
繼續(xù)加強(qiáng)醫(yī)療器械基本注冊(cè)能力建設(shè)。繼續(xù)實(shí)施標(biāo)準(zhǔn)完善計(jì)劃,不斷完善醫(yī)療器械標(biāo)準(zhǔn)體系,加強(qiáng)分類(lèi)命名和編碼工
作,加強(qiáng)法規(guī)的宣傳貫徹,大力開(kāi)展監(jiān)管科學(xué)研究,加強(qiáng)國(guó)際交流和合作。
不斷提高醫(yī)療器械注冊(cè)管理水平。規(guī)范地方注冊(cè)備案業(yè)務(wù),完善審批機(jī)制,完善國(guó)家辦器械審評(píng)中心管理,加強(qiáng)臨床試
驗(yàn)機(jī)構(gòu)和試驗(yàn)項(xiàng)目管理,嚴(yán)厲懲治違法違規(guī)行為。
編碼工作是管理醫(yī)療器械行業(yè)的關(guān)鍵工作。醫(yī)療器械編碼對(duì)該行業(yè)的許多方面產(chǎn)生了深遠(yuǎn)的影響。據(jù)賽博藍(lán)觀察,首批
15家醫(yī)療器械唯一標(biāo)識(shí)示范單位上線,包括注冊(cè)商、生產(chǎn)企業(yè)和運(yùn)營(yíng)商。形成了以點(diǎn)為先、以區(qū)擴(kuò)區(qū)的全國(guó)格局。
信號(hào)三:開(kāi)展風(fēng)險(xiǎn)隱患排查整治
持續(xù)加強(qiáng)疫情防控醫(yī)療器械監(jiān)管。加強(qiáng)對(duì)疫情防控醫(yī)療器械生產(chǎn)和經(jīng)營(yíng)使用環(huán)節(jié)監(jiān)管,加大對(duì)疫情防控醫(yī)療器械抽檢力
度。
不斷加強(qiáng)監(jiān)督檢查檢驗(yàn)和監(jiān)測(cè)評(píng)價(jià)。持續(xù)開(kāi)展飛行檢查,強(qiáng)化質(zhì)量監(jiān)督抽檢,加強(qiáng)不良事件監(jiān)測(cè)。持續(xù)加大違法案件查
處力度,嚴(yán)懲重處醫(yī)療器械違法違規(guī)行為。
持續(xù)加強(qiáng)監(jiān)管能力建設(shè)。完善醫(yī)療器械法規(guī)體系,加強(qiáng)法規(guī)宣傳培訓(xùn),強(qiáng)化檢查員隊(duì)伍和信息系統(tǒng)建設(shè),加強(qiáng)監(jiān)管科學(xué)
研究,推進(jìn)社會(huì)共治。
免責(zé)聲明:帶有本公司標(biāo)識(shí)的圖片未經(jīng)授權(quán)轉(zhuǎn)載,將追究法律責(zé)任;文章部分文字、圖片,視頻提及來(lái)源于網(wǎng)絡(luò),如有侵權(quán),請(qǐng)聯(lián)系刪除,版權(quán)歸原作者所有。

 首宏業(yè)務(wù)咨詢(xún)
首宏業(yè)務(wù)咨詢(xún)
 官方公眾號(hào)
官方公眾號(hào)
青島總部:山東省青島市市南區(qū)南京路 8 號(hào)府都大廈16 、20-22層
首宏醫(yī)療控股集團(tuán)股份有限公司 地址:山東省青島市南區(qū)南京路8號(hào)府都大廈 16、20-22 層 聯(lián)系電話:400-699-8388
Copyright @ 2018 Safehigh ALL Right Reserved.
ICP備案:魯ICP備19047490號(hào)-1